Perbedaan Utama – Geometri Elektron vs Geometri Molekul. Geometri suatu molekul menentukan reaktivitas, polaritas, dan aktivitas biologis dari molekul itu. Geometri suatu molekul dapat diberikan sebagai geometri elektron atau geometri molekul.
Teori VSEPR (teori Valence Shell Electron Pair Repulsion) dapat digunakan untuk menentukan geometri molekul. Geometri elektron mencakup pasangan elektron bebas yang ada dalam suatu molekul. Geometri molekuler dapat ditentukan dengan jumlah ikatan yang dimiliki molekul tertentu.
Perbedaan utama antara geometri elektron dan geometri molekul adalah bahwa geometri elektron ditemukan dengan mengambil pasangan elektron bebas dan ikatan dalam molekul sedangkan geometri molekul ditemukan hanya menggunakan ikatan yang ada dalam molekul.
Pengertian Geometri Elektron
Geometri elektron adalah bentuk molekul yang diprediksi dengan mempertimbangkan pasangan elektron ikatan dan pasangan elektron bebas. Teori VSEPR menyatakan bahwa pasangan elektron yang terletak di sekitar atom tertentu saling tolak. Pasangan elektron ini dapat berupa elektron ikatan atau elektron tidak berikatan.
Geometri elektron memberikan pengaturan spasial dari semua ikatan dan pasangan elektron bebas. Geometri elektron dapat diperoleh dengan menggunakan teori VSEPR.
Cara Menentukan Elektron Geometri
Berikut ini adalah langkah-langkah yang digunakan dalam menentukan geometri elektron.
- Memprediksi atom pusat molekul. Itu harus menjadi atom yang paling elektronegatif.
- Tentukan jumlah elektron valensi dalam atom pusat.
- Tentukan jumlah elektron yang disumbangkan oleh atom lain.
- Hitung jumlah elektron total di sekitar atom pusat.
- Bagilah angka itu dari 2. Ini memberikan jumlah gugus elektron yang ada.
- Kurangi jumlah ikatan tunggal yang ada di sekitar atom pusat dari jumlah sterik yang diperoleh di atas. Ini memberikan jumlah pasangan elektron bebas yang ada dalam molekul.
- Tentukan geometri elektron.
Contoh Geometri Elektron
Geometri Elektron dari CH4
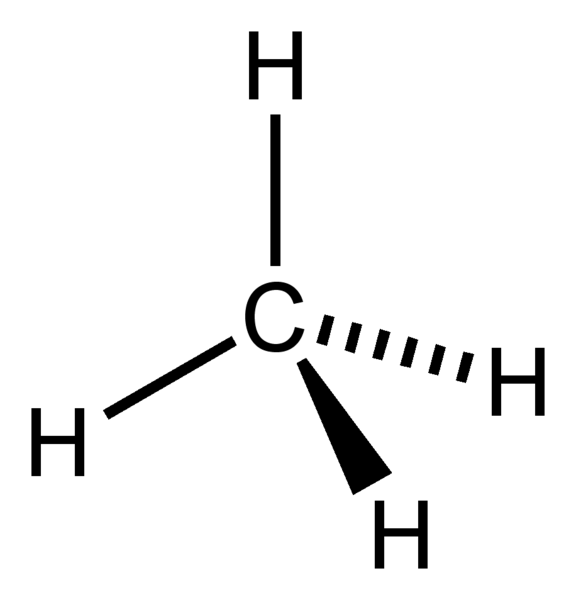
Atom pusat molekul = C
Jumlah elektron valensi C = 4
Jumlah elektron yang disumbangkan oleh atom hidrogen = 4 x (H)
= 4 x 1 = 4
Total jumlah elektron sekitar C = 4 + 4 = 8
Jumlah gugus elektron = 8/2 = 4
Jumlah ikatan tunggal hadir = 4
Jumlah pasangan elektron bebas = 4 – 4 = 0
Oleh karena itu, geometri elektron = tetrahedral
Geometri Elektron dari AlCl3
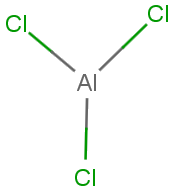
Atom pusat molekul = Al
Jumlah elektron valensi Al = 3
Jumlah elektron yang disumbangkan oleh atom Cl = 3 x (Cl)
= 3 x 1 = 3
Total jumlah elektron sekitar N = 3 + 3 = 6
Jumlah gugus elektron = 6/2 = 3
Jumlah ikatan tunggal hadir = 3
Jumlah pasangan elektron bebas = 3 – 3 = 0
Oleh karena itu, geometri elektron = planar trigonal
Terkadang, geometri elektron dan geometri molekul adalah sama. Itu karena hanya elektron ikatan yang dipertimbangkan dalam penentuan geometri tanpa adanya pasangan elektron tunggal.
Pengertian Geometri Molekul
Geometri molekul adalah bentuk molekul yang diprediksi dengan mempertimbangkan hanya pasangan elektron ikatan. Dalam hal ini, pasangan elektron bebas tidak diperhitungkan. Selain itu, ikatan rangkap dan rangkap tiga dianggap sebagai ikatan tunggal.
Geometri ditentukan berdasarkan fakta bahwa pasangan elektron bebas membutuhkan lebih banyak ruang daripada pasangan elektron ikatan. Misalnya, jika molekul tertentu terdiri dari dua pasang elektron ikatan bersama dengan pasangan elektron bebas, geometri molekulnya tidak linier. Geometri ada “bengkok atau sudut” karena pasangan elektron bebas membutuhkan lebih banyak ruang daripada dua pasangan elektron ikatan.
Contoh Geometri Molekul
Geometri Molekul H2O
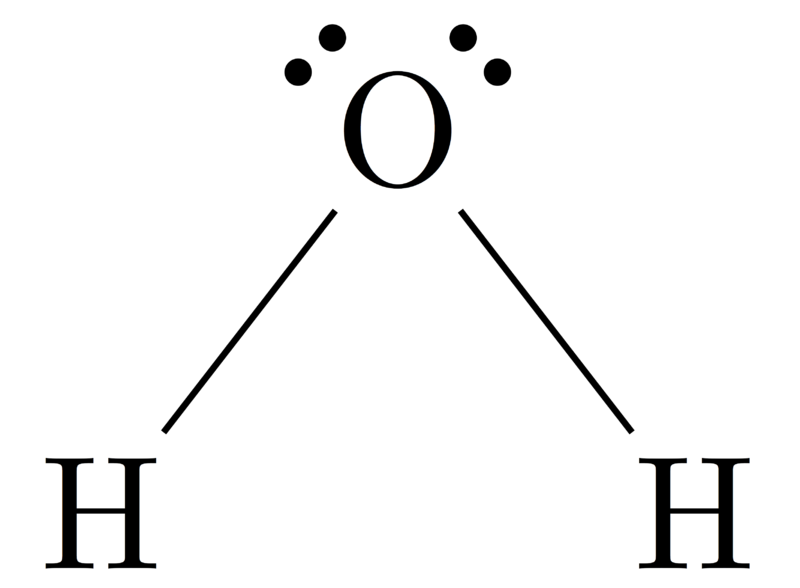
Atom pusat molekul = O
Jumlah elektron valensi O = 6
Jumlah elektron yang disumbangkan oleh atom hidrogen = 2 x (H)
= 2 x 1 = 2
Total jumlah elektron sekitar N = 6 + 2 = 8
Jumlah gugus elektron = 8/2 = 4
Jumlah pasangan elektron bebas = 2
Jumlah ikatan tunggal sekarang = 4 – 2 = 2
Oleh karena itu, geometri elektron = Bent
Geometri Molekul Amonia (NH3)
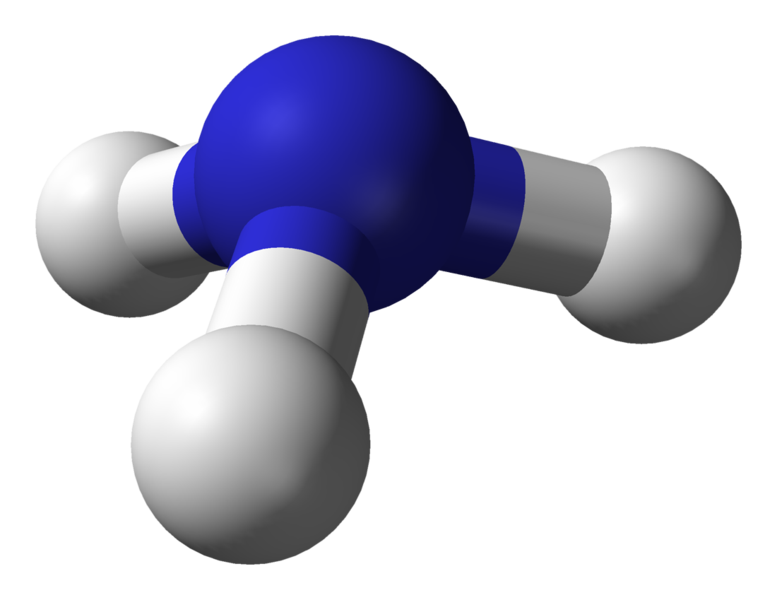
Atom pusat molekul = N
Jumlah elektron valensi N = 5
Jumlah elektron yang disumbangkan oleh atom hidrogen = 3 x (H)
= 3 x 1 = 3
Total jumlah elektron sekitar N = 5 + 3 = 8
Jumlah gugus elektron = 8/2 = 4
Jumlah pasangan elektron bebas = 1
Jumlah ikatan tunggal hadir = 4 – 1 = 3
Oleh karena itu, geometri elektron = piramida trigonal
Perbedaan Antara Geometri Elektron dan Geometri Molekul
Definisi
- Geometri Elektron: Geometri elektron adalah bentuk molekul yang diprediksi dengan mempertimbangkan pasangan elektron ikatan dan pasangan elektron bebas.
- Geometri Molekul: Geometri molekul adalah bentuk molekul yang diprediksi dengan mempertimbangkan hanya pasangan elektron ikatan.
Pasangan elektron bebas
- Geometri Elektron: Pasangan elektron bebas dipertimbangkan ketika menemukan geometri elektron.
- Geometri Molekuler: Pasangan elektron bebas tidak dipertimbangkan ketika menemukan geometri molekul.
Jumlah Pasangan Elektron
- Geometri Elektron: Jumlah pasangan elektron total harus dihitung untuk menemukan geometri elektron.
- Geometri Molekuler: Jumlah pasangan elektron pengikat harus dihitung untuk menemukan geometri molekul.
Kesimpulan
Geometri elektron dan geometri molekul adalah sama ketika tidak ada pasangan elektron tunggal pada atom pusat. Tetapi jika ada pasangan elektron tunggal pada atom pusat, geometri elektron selalu berbeda dari geometri molekul. Oleh karena itu, perbedaan antara geometri elektron dan geometri molekul tergantung pada pasangan elektron bebas yang ada dalam molekul.

