Perbedaan Utama – Senyawa Organik vs Anorganik. Senyawa organik dan anorganik adalah dua kategori luas senyawa dalam kimia. Hampir semua teori, hukum, dan hipotesis dalam bidang kimia dibuat berdasarkan senyawa organik dan anorganik. Kedua jenis ini tersusun dari materi dalam keadaan fisik apa pun: keadaan padat, keadaan cair atau keadaan gas.
Sifat umum dari Senyawa Organik dan Anorganik:
| Senyawa organik | Senyawa anorganik |
| Banyak gas, cairan atau padatan | Sebagian besar adalah padatan |
| Biasanya selalu mengandung karbon, terutama ikatan karbon-hidrogen | Mungkin mengandung karbon. Berisi logam dan elemen lainnya. Tidak mengandung ikatan karbon-hidrogen. |
| Umumnya ditemukan pada makhluk hidup, yaitu hewan dan tumbuhan. | Umumnya diperoleh dari benda mati, yaitu mineral. |
| Secara biologis | Mineral di alam |
| Beberapa senyawa sangat kompleks dan memiliki massa molekul tinggi. Senyawa kompleks ini stabil. | Senyawa anorganik kurang kompleks. Secara komparatif senyawa kompleks umumnya kurang stabil. |
| Membentuk ikatan kovalen
|
Sebagian besar membentuk ikatan ionik, beberapa ikatan kovalen hadir |
| Terdiri dari beberapa elemen saja, umumnya karbon, hidrogen, oksigen, nitrogen, belerang, dan fosfor | Terdiri dari semua elemen yang dikenal |
| Tidak dapat membuat garam karena kovalen karbon | Membuat garam |
| Titik leleh dan titik didih yang lebih rendah | Titik lebur dan titik didih yang lebih tinggi |
| Tidak larut dalam air, larut dalam pelarut organik | Mudah larut dalam air, tidak larut dalam pelarut organik |
| Sangat mudah terbakar dan tidak stabil | Tidak mudah terbakar dan tidak mudah menguap |
| Konduktor panas dan listrik yang lebih buruk dalam larutan air | Konduktor panas dan listrik yang lebih baik dalam larutan air |
| Laju reaksi lebih lambat | Laju reaksi lebih tinggi |
| Menghasilkan rangkaian produk yang lebih kompleks selama reaksi | Menghasilkan rangkaian produk yang kurang kompleks selama reaksi |
| Peragakan fenomena isomerisme | Hanya senyawa koordinasi yang menunjukkan fenomena isomerisme |
| Dikelompokkan ke dalam banyak kelas berdasarkan kelompok fungsional, yang dikenal sebagai seri homolog. Setiap kelas diwakili oleh rumus umum dan anggota menunjukkan properti yang serupa. | Dikelompokkan sebagai asam, basa dan garam. Tidak ada seri homolog ditemukan |
| Termasuk asam nukleat, lemak, gula, protein, enzim dan banyak bahan bakar. | Termasuk garam, logam, zat yang terbuat dari unsur tunggal dan senyawa lain yang tidak mengandung karbon yang terikat pada hidrogen. |
| Contoh: metana, etana, asetilena, alkohol, karbon tetraklorida (CCl4), urea [CO (NH2) 2] | Contoh: karbon dioksida, asam sulfat, NaCl, berlian (karbon murni) |
Perbedaan utama antara senyawa organik dan anorganik adalah bahwa senyawa organik pada dasarnya memiliki satu atau lebih atom karbon dalam strukturnya sedangkan senyawa anorganik mungkin atau mungkin tidak memiliki atom karbon.
Pengertian Senyawa Organik
Senyawa organik adalah senyawa yang pada dasarnya memiliki satu atau lebih atom karbon, terikat secara kovalen dengan unsur-unsur lain. Paling umum, atom karbon ini terikat pada atom hidrogen, oksigen, dan nitrogen. Konsep senyawa organik mungkin membingungkan pada beberapa titik seperti dalam kasus karbon dioksida (CO2).
Meskipun CO2 memiliki atom karbon yang terikat pada dua atom oksigen, CO2 tidak dianggap sebagai senyawa organik karena alasan historis. Senyawa seperti karbonat, sianida, CO dan CO2 ditemukan sebelum penemuan senyawa organik. Pada saat itu, ini dianggap sebagai senyawa anorganik, dan praktik ini masih berlanjut.
Kimia organik adalah cabang kimia yang menjelaskan struktur, sifat, reaksi, dan fakta penting lainnya tentang senyawa organik. Kimia organik adalah subjek yang rumit dan para ilmuwan menggunakannya untuk menciptakan sejumlah produk berharga. Karena hampir semua organisme terdiri dari molekul organik, senyawa organik sangat penting untuk kehidupan di bumi.
Karena ada sejumlah berbagai senyawa yang termasuk dalam kategori senyawa organik, senyawa ini dapat diklasifikasikan lebih lanjut dalam berbagai cara. Jenis senyawa organik yang paling umum adalah hidrokarbon. Hidrokarbon juga dapat diklasifikasikan dalam berbagai cara karena senyawa ini memiliki struktur, sifat yang berbeda, dan menunjukkan reaksi yang berbeda.
Polimer adalah jenis lain dari senyawa organik penting. Meskipun beberapa polimer terdiri dari tulang punggung anorganik, mereka juga mengandung gugus organik dan disebut polimer hibrida. Polimer digunakan dalam berbagai aplikasi dan proses yang penting dalam kehidupan sehari-hari.
Senyawa organik seperti hidrokarbon dapat diklasifikasikan sebagai alifatik dan aromatik berdasarkan ada tidaknya struktur cincin aromatik. Senyawa organik ditemukan di ketiga kondisi fisik dalam suhu kamar. Sebagai contoh,
- Fase padat – beberapa amida
- Fase cair – alkohol seperti etanol
- Fasa gas – gas seperti metana
Contoh Senyawa Organik
Molekul yang terkait dengan organisme hidup adalah organik. Ini termasuk asam nukleat, lemak, gula, protein, enzim, dan bahan bakar hidrokarbon. Semua molekul organik mengandung karbon, hampir semua mengandung hidrogen, dan banyak pula yang mengandung oksigen.
- DNA
- Gula meja atau sukrosa, C12H22O11
- Benzena, C6H6
- Metana, CH4
- Etanol atau alkohol gandum, C2H6O
Pengertian Senyawa Anorganik
Senyawa anorganik adalah senyawa apa pun yang bukan merupakan senyawa organik. Dengan kata lain, senyawa anorganik pada dasarnya tidak tersusun dari atom karbon. Bisa ada atom karbon yang ada atau tidak ada.
Kimia anorganik adalah cabang kimia yang menjelaskan struktur, perilaku, sifat, dan karakteristik senyawa anorganik. Senyawa anorganik terutama ditemukan sebagai mineral, senyawa yang terikat logam atau senyawa organologam.

Karena banyak senyawa anorganik terdiri dari logam atau ion logam, mereka mampu menghantarkan listrik. Beberapa senyawa anorganik dapat menghantarkan listrik bahkan tanpa logam seperti grafit. Sebagian besar senyawa anorganik memiliki ikatan ionik dan ikatan kovalen. Banyak senyawa anorganik juga sangat berwarna karena adanya elemen blok d.
Sebagian besar senyawa anorganik larut dalam air karena ikatan ioniknya. Ini dapat terpecah menjadi ion mereka ketika ditambahkan ke air. Properti penting lainnya adalah kemampuan mereka untuk membentuk kristal. Kemampuan ini juga disebabkan oleh sifat ikatan mereka.
Contoh Senyawa Anorganik
Anorganik meliputi garam, logam, zat yang terbuat dari unsur tunggal dan senyawa lain yang tidak mengandung karbon yang terikat pada hidrogen. Beberapa molekul anorganik memang mengandung karbon.
- Garam meja atau natrium klorida, NaCl
- Karbon dioksida, CO2
- Berlian (karbon murni)
- Perak
- Belerang
Perbedaan Antara Senyawa Organik dan Anorganik
Definisi
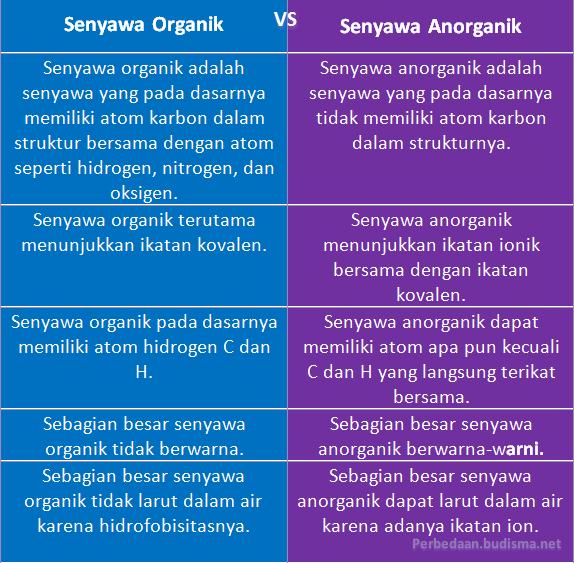
- Senyawa organik: Senyawa organik adalah senyawa yang pada dasarnya memiliki atom karbon dalam struktur bersama dengan atom seperti hidrogen, nitrogen, dan oksigen.
- Senyawa anorganik: Senyawa anorganik adalah senyawa yang pada dasarnya tidak memiliki atom karbon dalam strukturnya.
Jenis Ikatan
- Senyawa organik: Senyawa organik terutama menunjukkan ikatan kovalen.
- Senyawa anorganik: Senyawa anorganik menunjukkan ikatan ionik bersama dengan ikatan kovalen.
Atom Hadir
- Senyawa organik: Senyawa organik pada dasarnya memiliki atom hidrogen C dan H.
- Senyawa anorganik: Senyawa anorganik dapat memiliki atom apa pun kecuali C dan H yang langsung terikat bersama.
Penampilan
- Senyawa organik: Sebagian besar senyawa organik tidak berwarna.
- Senyawa anorganik: Sebagian besar senyawa anorganik berwarna-warni.
Kelarutan dalam air
- Senyawa organik: Sebagian besar senyawa organik tidak larut dalam air karena hidrofobisitasnya.
- Senyawa anorganik: Sebagian besar senyawa anorganik dapat larut dalam air karena adanya ikatan ion.
Kesimpulan
Bidang utama kimia termasuk Kimia Organik, Kimia Anorganik, Kimia Fisik dan Kimia Analitik. Di antaranya, kimia organik berperan dalam struktur, sifat, dan reaksi senyawa organik. Kimia anorganik adalah bidang yang menjelaskan struktur, sifat, dan reaksi senyawa anorganik. Dengan demikian, perbedaan antara kimia organik dan anorganik berasal dari perbedaan antara senyawa organik dan anorganik, yang pada gilirannya, tergantung pada ada atau tidak adanya atom karbon dalam struktur mereka.

