Perbedaan utama: Elektronegativitas adalah sifat kimia yang menentukan kecenderungan suatu atom untuk menarik elektron dalam ikatan kovalen. Ini adalah properti yang tidak dapat diukur secara langsung. Afinitas elektron suatu atom adalah jumlah energi yang diberikan oleh atom ketika sebuah elektron ditambahkan atom netral atau molekul untuk membuatnya menjadi ion negatif. Dalam fisika keadaan padat, afinitas elektron juga dikenal sebagai energi yang diperlukan untuk memindahkan elektron dari dasar pita konduksi terendah ke keadaan stasioner dalam ruang hampa udara terdekat.
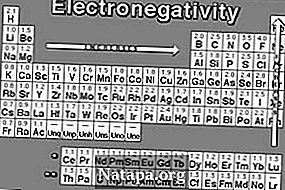
Elektronegativitas dan Afinitas Elektron adalah dua istilah berbeda yang ditemukan orang ketika berhadapan dengan atom dan ikatan. Ilmu pengetahuan dasar mengajarkan kita bahwa atom membuat ikatan dengan meminjam elektron, memberikan elektron atau berbagi elektron. Elektron ini bertanggung jawab untuk membentuk banyak hal berbeda yang kita ketahui dan gunakan dalam kehidupan sehari-hari termasuk kebutuhan dasar seperti air. Ketika kita berbicara tentang ikatan, elektronegativitas dan afinitas elektron memainkan peran besar. Kedua istilah ini sering membingungkan karena kesamaan mereka tetapi dalam kenyataannya, mereka merujuk pada dua hal yang berbeda dan memiliki banyak perbedaan.
Elektronegativitas adalah sifat kimia yang menentukan kecenderungan suatu atom untuk menarik elektron dalam ikatan kovalen. Ini adalah sifat yang tidak dapat diukur secara langsung dan dipengaruhi oleh nomor atom atom dan jarak tempat elektron valensinya berada dari inti yang bermuatan. Karenanya, semakin tinggi keelektronegatifan suatu senyawa atau unsur, semakin ia menarik elektron ke arahnya. Konsep elektronegativitas diajukan oleh Linus Pauling pada tahun 1932 sebagai tambahan pada teori ikatan valensi. Karena keelektronegatifan tidak dapat diukur secara langsung, ia dihitung menggunakan sifat atom dan molekul atom seperti muatan nuklir dan jumlah / lokasi elektron lain yang ada dalam kulit atom.

Afinitas elektron suatu atom adalah jumlah energi yang diberikan oleh atom ketika sebuah elektron ditambahkan atom netral atau molekul untuk membuatnya menjadi ion negatif. Dalam fisika keadaan padat, afinitas elektron juga dikenal sebagai energi yang diperlukan untuk memindahkan elektron dari dasar pita konduksi terendah ke keadaan stasioner dalam ruang hampa udara terdekat. Ketika sebuah elektron ditambahkan ke atom atau molekul, semakin banyak energi yang dilepaskan, semakin mudah sebuah atom menjadi ion.Afinitas elektron adalah sifat yang dapat diukur dengan mudah menggunakan langkah-langkah ilmiah seperti energi yang dilepaskan setelah elektron ditambahkan.
Meskipun mereka mirip satu sama lain dan mengukur kecenderungan atom untuk menarik elektron; mereka menanggung sedikit perbedaan. Satu perbedaan utama adalah bahwa konsep elektronegativitas tidak dapat diukur dan terutama digunakan untuk menjelaskan ikatan kovalen dan polaritas ikatan. Namun, afinitas elektron dapat diukur dan dapat dengan mudah diukur dengan mengukur jumlah energi yang dilepaskan ketika elektron ditambahkan. Keelektronegatifan juga membantu memahami lokasi pasangan elektron ikatan. Penawaran keelektronegatifan dengan masing-masing atom, sedangkan afinitas elektron berhubungan dengan atom dalam suatu molekul. Elektronegativitas juga merupakan sifat, sedangkan afinitas elektron adalah ukuran. Nilai keelektronegatifan juga dapat berubah tergantung pada molekul yang terikat padanya, sedangkan afinitas elektron tidak berubah.
